Валентность в химии – это свойство атомов образовывать химические связи с другими атомами. Она определяет, сколько электронов может участвовать в образовании связей и, следовательно, сколько атомов может соединить. Валентность является важным понятием в химии, так как она позволяет предсказывать тип и количество связей, которые может образовать атом.
Однако в некоторых случаях атомы могут образовывать разные виды связей, что называется переменной валентностью. Это означает, что атом может образовывать связи с разным количеством электронов и иметь разное количество связывающих атомов. Переменная валентность может быть обусловлена различными факторами, такими как электронная конфигурация и окружение атома.
Примером переменной валентности является железо, которое может иметь валентность +2 и +3. В соединениях с валентностью +2 железо образует две связи, а соединения с валентностью +3 – три связи. Это приводит к образованию различных соединений железа с разными свойствами.
Кроме железа, переменную валентность могут иметь и другие элементы, такие как медь, хром, ртуть и многие другие. Это позволяет им образовывать различные типы соединений и обладать разными химическими свойствами. Изучение переменной валентности важно для понимания химических процессов и применения валентности в химической номенклатуре и формулах соединений.
Понятие переменной валентности в химии: примеры и определение
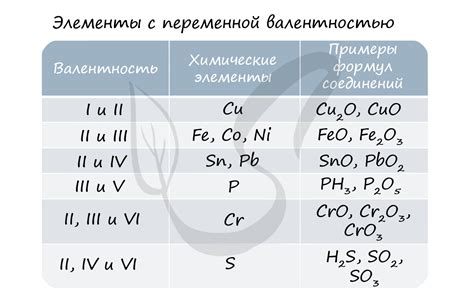
Под переменной валентностью в химии понимается способность химического элемента изменять свою валентность, то есть число электронов, которые он может принять или отдать при образовании химических связей с другими элементами. Валентность химического элемента указывает на количество связей, которые он способен образовать.
Переменная валентность является характеристикой переходных металлов, у которых электросостояние внешней электронной оболочки может меняться. К примеру, железо может иметь две валентности: Fe^2+ и Fe^3+. Куприй может иметь две валентности: Cu^+ и Cu^2+, а марганец может иметь четыре валентности: Mn^2+, Mn^3+, Mn^4+ и Mn^7+.
Переменная валентность позволяет элементам образовывать соединения с разными степенями окисления. Например, соединение FeCl2 содержит железо с валентностью Fe^2+, а соединение FeCl3 содержит железо с валентностью Fe^3+. Это все возможно благодаря тому, что электроны внешней электронной оболочки переходного металла могут находиться в разных энергетических состояниях.
Переменная валентность имеет большое значение в ионных соединениях, где валентность элемента указывается рядом с его знаком, а также в органической химии, где она может использоваться для описания сложных органических соединений.
Что такое переменная валентность?
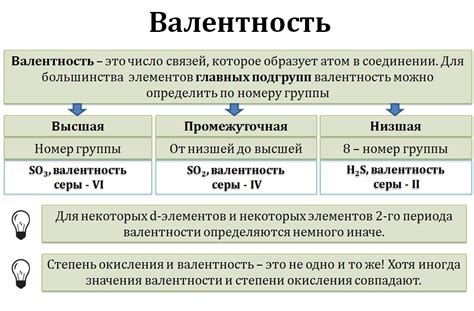
Переменная валентность - это свойство химических элементов проявлять различную степень окисления в различных соединениях. Оно связано с тем, что у элемента может быть несколько различных электроотрицательностей.
Электроотрицательность - важный параметр, который определяет способность атома притягивать электроны. В зависимости от электроотрицательности элемента он может принимать разное количество электронов при образовании химических связей. Это и определяет переменную валентность.
Например, у металлов, таких как железо или медь, валентность может варьироваться от 2 до 3 или от 1 до 2 соответственно. Кислород может иметь валентность -2 или -1, в зависимости от контекста.
Переменная валентность играет важную роль в химических реакциях и образовании соединений. Благодаря этому свойству элемента возможно множество вариаций химических соединений с участием одного и того же элемента.
Для наглядности валентность элементов часто указывается в римской цифровой системе. Например, железо (Fe) может иметь валентность II или III, а серебро (Ag) - I или II.
Примеры переменной валентности в химии
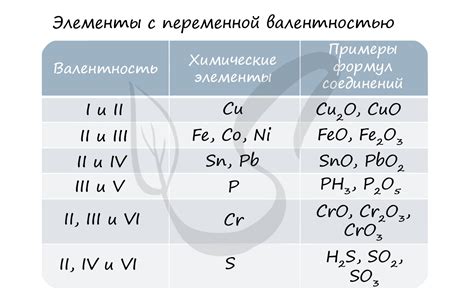
Переменная валентность в химии является особенностью некоторых элементов, которые способны проявлять несколько различных степеней окисления в различных химических соединениях. Ниже приведены некоторые примеры элементов с переменной валентностью:
Марганец (Mn): Варьирует валентность от +2 до +7. Например, в соединении MnO2 марганец имеет валентность +4, а в KMnO4 - +7.
Железо (Fe): Имеет валентность от -2 до +6. Например, в соединении FeO железо имеет валентность +2, а в Fe2O3 - +3.
Серебро (Ag): Может проявлять валентность +1 или +2. Например, в Ag2O серебро имеет валентность +1, а в AgCl - +2.
Олово (Sn): Варьирует валентность от -4 до +4. Например, в SnO2 олово имеет валентность +4, а в SnCl2 - +2.
Это лишь несколько примеров элементов с переменной валентностью в химии. Многие другие элементы, такие как сера (S), хром (Cr), медь (Cu) и др., также могут проявлять данное явление. Понимание переменной валентности позволяет ученным более точно определять состав и свойства химических соединений.
Особенности переменной валентности

Переменная валентность – это свойство химических элементов образовывать различные соединения с разными степенями окисления. Это свойство характерно для некоторых переходных металлов и ряда элементов с p-оболочкой.
Основные особенности переменной валентности:
- Множество окислительных состояний: Элементы с переменной валентностью могут образовывать соединения с разными степенями окисления. Например, железо может иметь окислительное состояние +2 или +3. Это обусловлено наличием свободных d-электронов в электронной оболочке элемента.
- Изменчивость валентности: Элементы с переменной валентностью могут изменять свою валентность в различных химических реакциях. Например, марганец может иметь валентность +4, +6 или +7 в различных соединениях.
- Сложность определения валентности: Валентность элементов с переменной валентностью не всегда легко определить, поскольку она зависит от конкретного соединения и условий реакции. Необходимо проводить анализ исходных и конечных соединений для определения степени окисления элемента.
- Влияние на химические свойства: Валентность элемента существенно влияет на его химические свойства и активность. Разные соединения с разной валентностью могут обладать разными физическими и химическими свойствами. Например, медь (I) характеризуется одними свойствами, а медь (II) – другими.
Изучение переменной валентности элементов является важным в химии, поскольку позволяет понять и объяснить множество явлений и реакций, происходящих в природе и промышленности. Кроме того, переменная валентность играет важную роль в разработке новых соединений и материалов с улучшенными свойствами.